You're one in a million. ~在茫茫蛋白海中,只為與你相遇~
西方墨點法(Western blot)是用於檢測混合物中特定蛋白質的分析技術,主要透過蛋白質大小分離、轉移至固態載體,並使用特異性抗體來標記與視覺化目標蛋白。

以下是進行西方墨點法實驗的完整步驟指南:
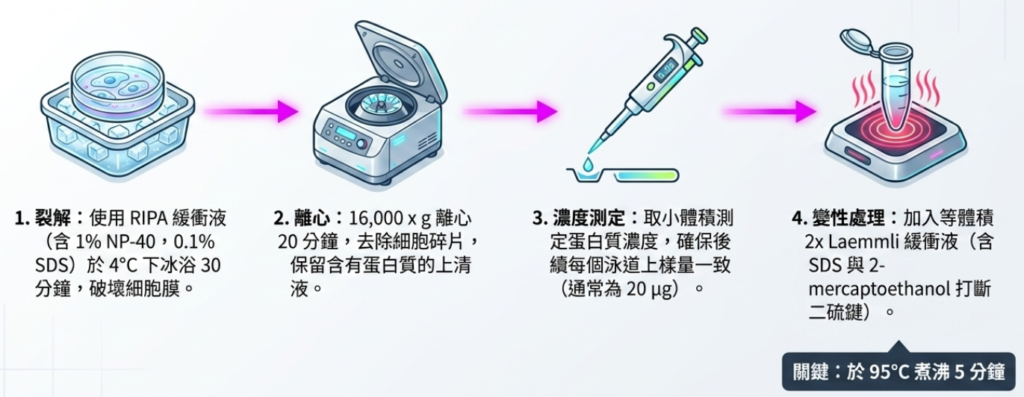
步驟一:樣本製備 (Sample Preparation) 良好的樣本製備是實驗成功的基礎,能確保蛋白質被充分萃取並防止其降解。
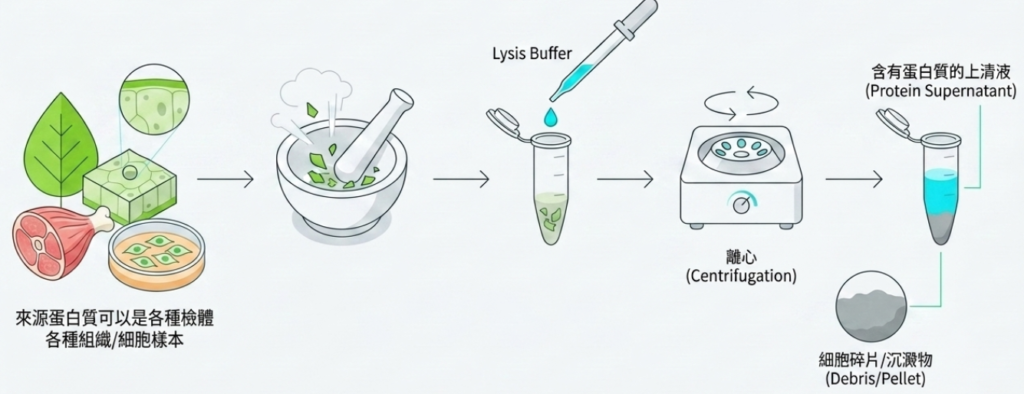
- 將細胞培養盤置於冰上,用冰的 Tris 緩衝鹽水(TBS)清洗細胞。
- 加入冰的 RIPA 裂解緩衝液(內含蛋白酶抑制劑),用冷塑膠刮刀刮下細胞並轉移至預冷的離心管中。
- 在 4°C 下持續搖動 30 分鐘;必要時可進行超音波震盪,以確保細胞完全破裂並降低樣本黏稠度。
- 在 4°C 預冷的離心機中,以 16,000 x g 離心 20 分鐘,隨後將上清液轉移至乾淨的管中。
- 進行蛋白質濃度測定分析。
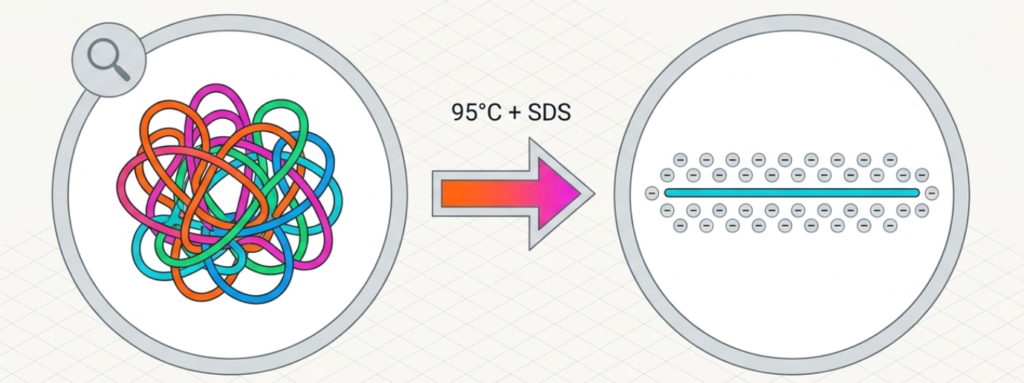
- 取等量蛋白質(例如 20 μg)加入等體積的 2x Laemmli 樣本加載緩衝液,然後在 95°C 下煮沸 5 分鐘使其變性。
步驟二:凝膠電泳 (Gel Electrophoresis) 此步驟利用 SDS-PAGE 依據蛋白質的分子量大小將其分離。

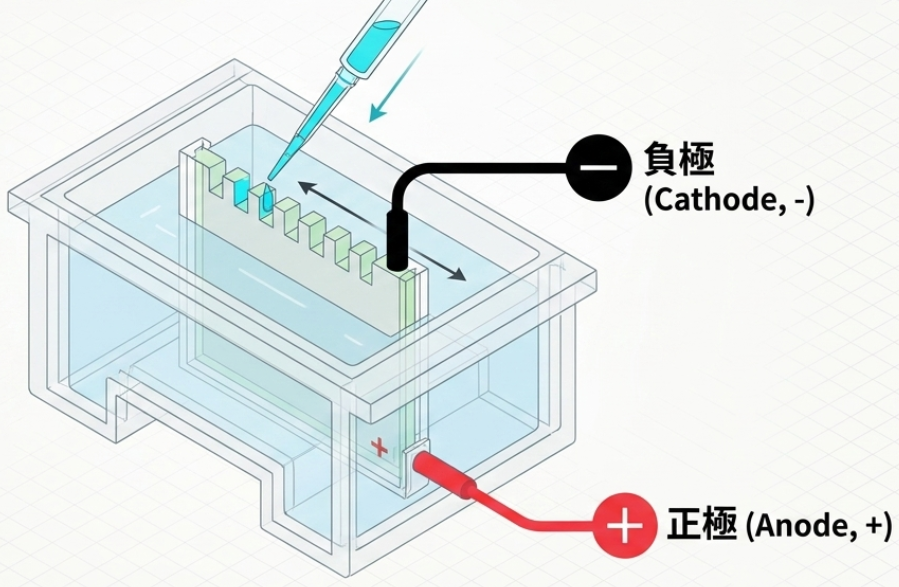

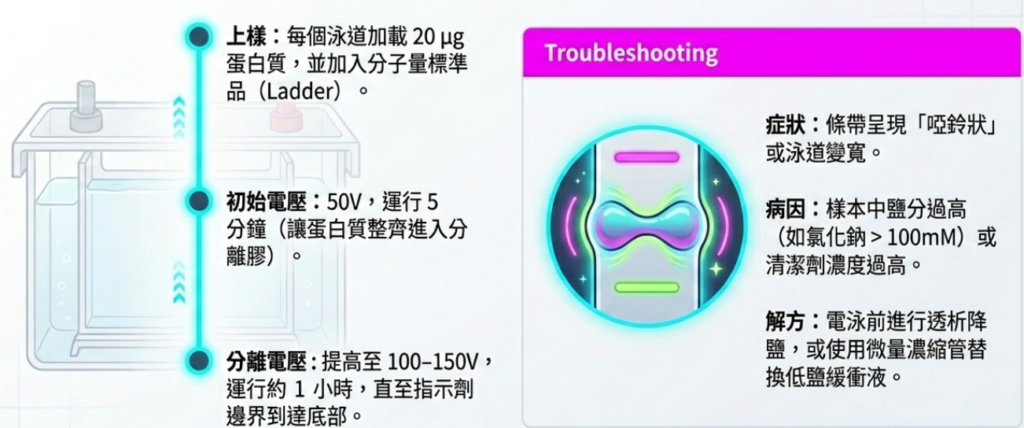
- 將等量的蛋白質樣本以及已知分子量的標記物(Ladder/Marker)載入 SDS-PAGE 凝膠的孔洞中。
- 先以 50 V 的電壓跑 5 分鐘,接著將電壓提高到 100–150 V,繼續跑約 1 小時直到完成。
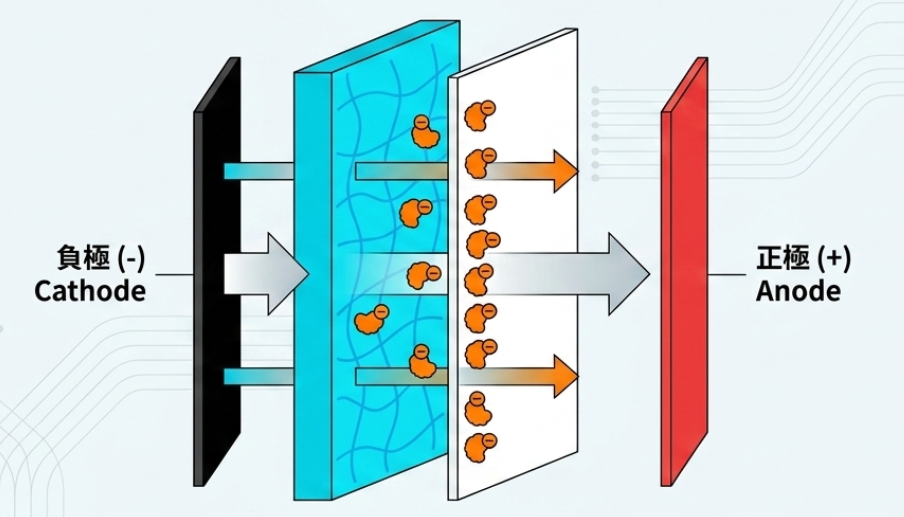
步驟三:蛋白質轉漬 (Transfer) 將凝膠內分離好的蛋白質轉移到膜上,以便後續與抗體結合。


- 常見的轉漬膜有 PVDF 膜或硝化纖維素(NC)膜,前者較為堅固且允許重複探測(Re-probing),使用前需先浸泡甲醇。
- 組裝轉漬三明治,若採用效果較穩定的濕式轉漬(Wet transfer),其順序為:海綿 > 濾紙 > 凝膠 > 膜 > 濾紙 > 海綿(皆需浸泡過轉漬緩衝液),並確保三明治中沒有殘留氣泡。
- 在冷房中以 10 mA 恆定電流轉漬隔夜,或以 100 V 轉漬 30 分鐘至 2 小時(視蛋白質大小而定,較大蛋白質需要較長轉漬時間)。
- 可短暫使用 Ponceau S 染液檢查膜上的蛋白質轉漬品質是否均勻。

步驟四:封閉 (Blocking) 為防止抗體在膜上發生非特異性結合(造成背景雜訊),必須進行封閉處理。
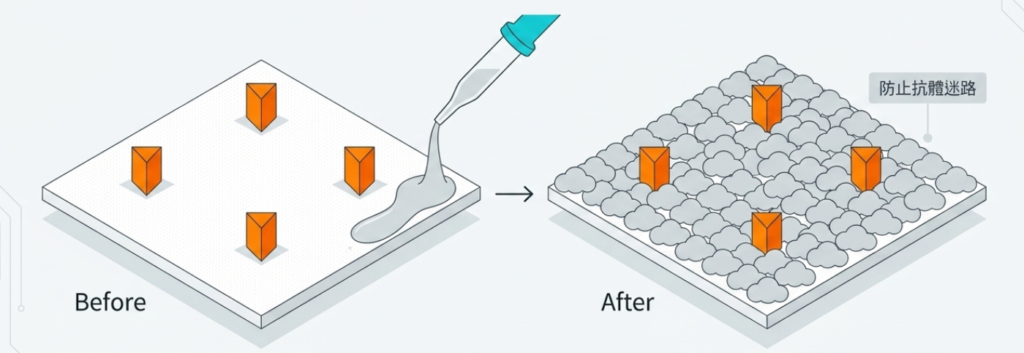

- 常用的封閉液包括含 3% BSA 或 5% 脫脂奶粉的 TBST(含有 Tween 20 的 Tris 緩衝鹽水)。
- 將膜浸泡於封閉液中,在室溫下搖動 1 小時。

HyBlock 1 min Blocking Buffer
脫脂奶粉
步驟五:抗體培育 (Antibody Incubation)
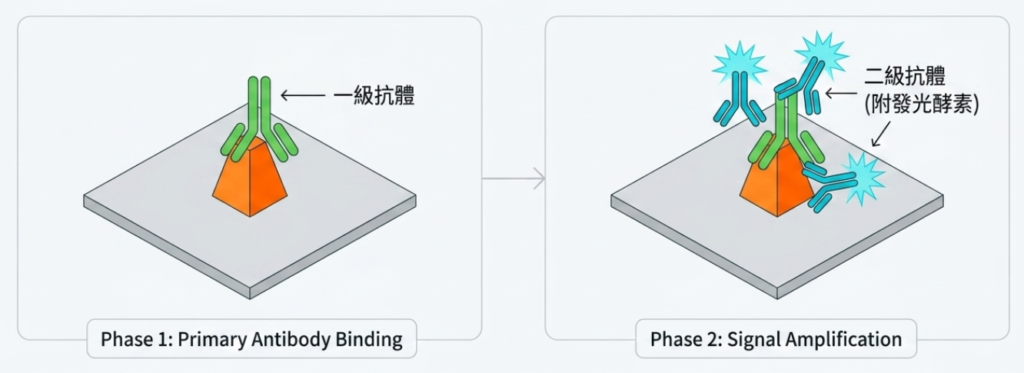
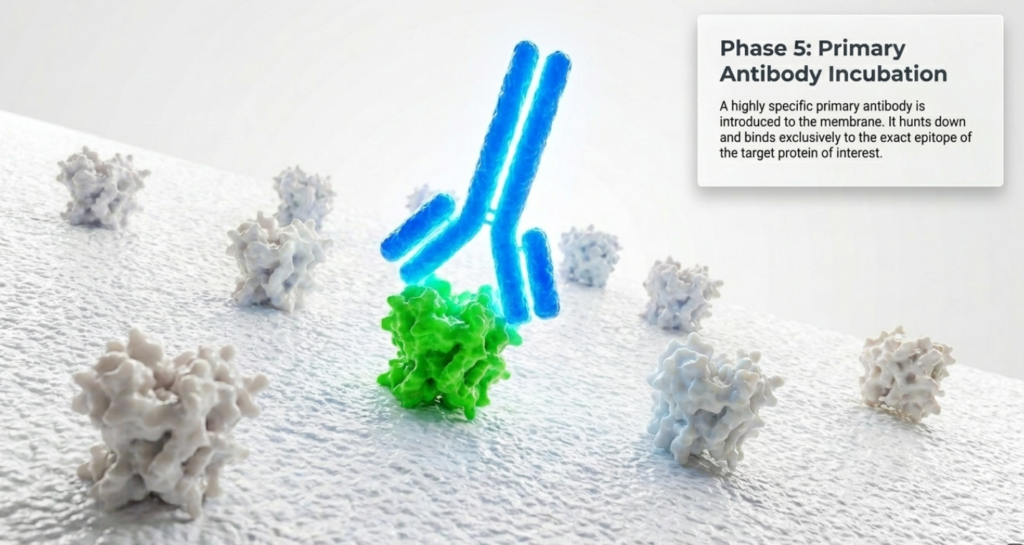
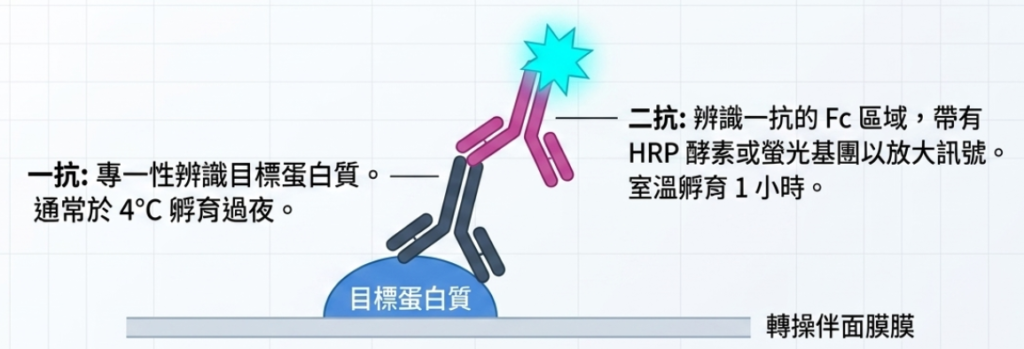
- 一抗培育: 選擇合適的一抗(避免使用與樣本同物種的宿主抗體以免交叉反應),根據建議比例稀釋於封閉液中,在 4°C 下培育隔夜(或室溫 1-3 小時)。
- 清洗: 用 TBST 清洗膜 3-5 次,每次 5 分鐘,以洗掉未結合的一抗。
- 二抗培育: 加入帶有 HRP(辣根過氧化物酶)等標記的二抗,以放大訊號。在室溫下培育 1 小時。
- 清洗: 再次用 TBST 洗滌膜 3-5 次,每次 5 分鐘。
步驟六:影像擷取 (Imaging)



- 依據製造商指示,將化學發光受質(Chemiluminescent substrate)滴加至膜上與 HRP 反應發光。
- 推薦使用數位 CCD 相機影像系統來擷取訊號,它具有比傳統 X 光底片更好的線性動態範圍,能避免高強度條帶過度飽和,且更利於後續的精確定量。

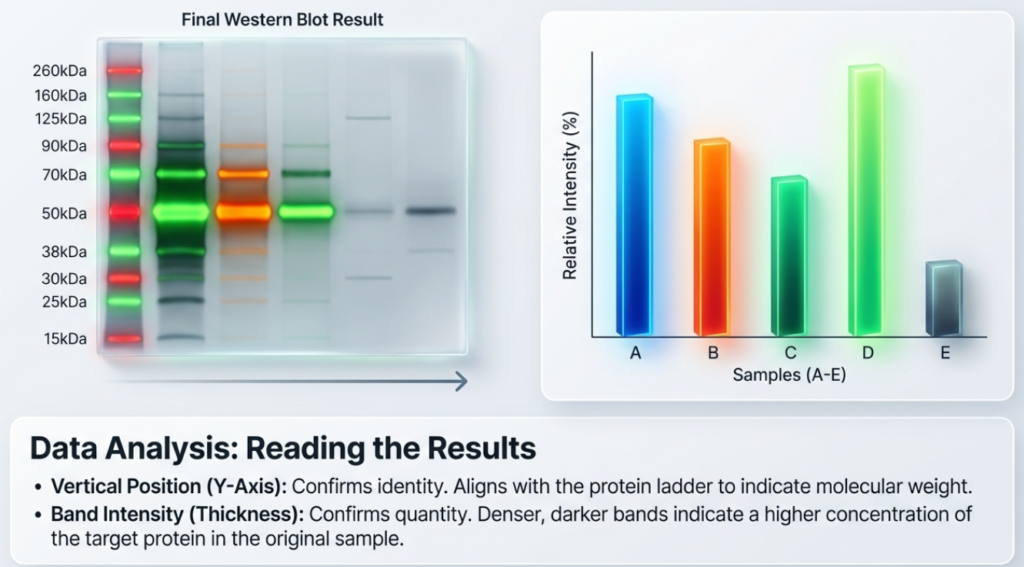
步驟七:數據分析與定量 (Data Analysis and Quantification)
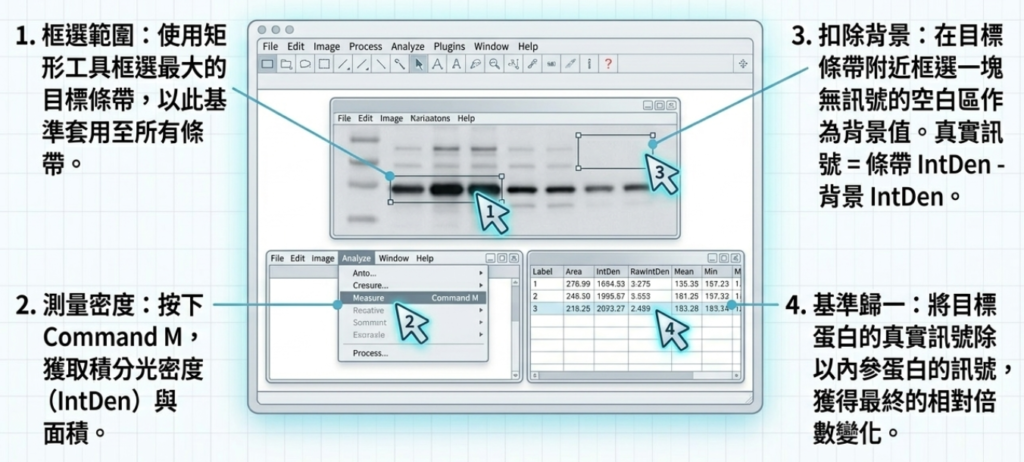
- 使用如 Image J 等影像分析軟體,圈選最大條帶的區域,讀取目標蛋白的訊號強度(IntDen),並務必扣除背景值。
- 進行校正(Normalization): 為了消弭加樣誤差與轉漬效率的差異,必須將目標蛋白的強度與「載入對照組」(如 GAPDH、β-actin 等持家蛋白)或「總蛋白質(Total Protein)」的強度相除,算出校正後的相對表現量。
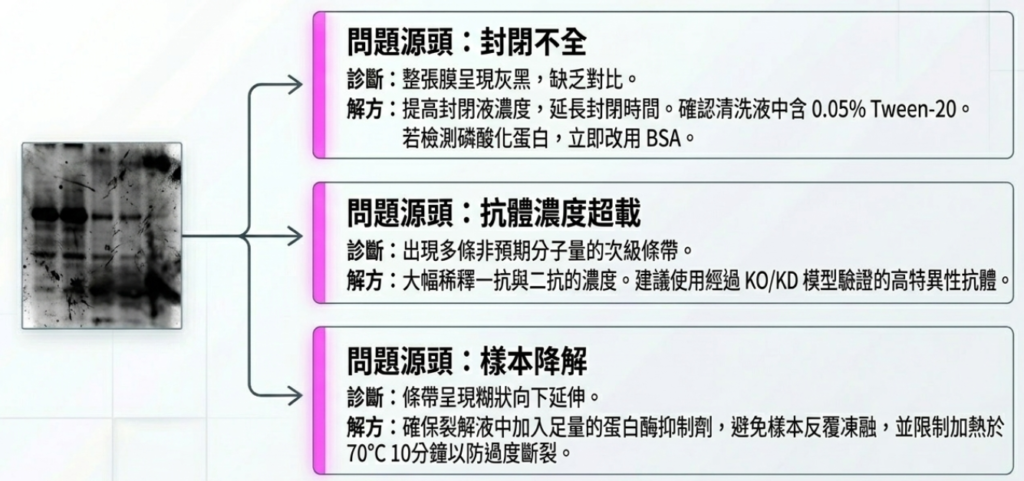
Trouble Shutting